精准调控神经活动对于深入理解神经系统功能以及开发神经疾病治疗方法具有重要意义,而光热转换材料与光活性有机半导体因其独特性质,已成为该领域的研究热点。尤其值得关注的是,光活性有机半导体中的体异质结(BHJ)在构建非遗传性、高精度柔性光神经调控器件中展现出巨大潜力,但目前仍面临BHJ与软组织之间界面适配性不足的挑战,这一问题制约了信号转导效率、组织粘附性能及生物相容性,亟待进一步解决。近日,生命学院姚骏实验室与化学系李景虹实验室、张昊实验室及电子工程系盛兴实验室合作,在纳米领域知名期刊《ACS Nano》连续发表论文,报道了联合团队在神经调控技术方面取得的创新突破,为神经系统疾病的治疗提供了新思路与方法。
(一)高度分支的Au超粒子:高效光热转换实现精准神经调控
清华大学化学系李景虹、张昊、生命学院姚骏、化学系瓮康康共同通讯团队聚焦于通过结构设计提升光热转换材料性能,成功设计出一种新型高效光热转换材料——高度分支的Au超粒子(3D Au superparticles),并利用其实现精准的神经活动控制。相关研究成果以“高支化金超粒子作为光学神经调节的高效光热传感器”(Highly Branched Au Superparticles as Efficient Photothermal Transducers for Optical Neuromodulation)为题在线发表于ACS Nano期刊。

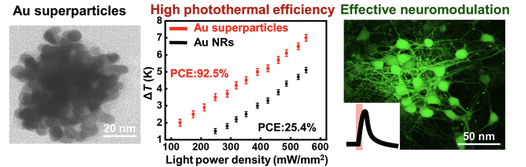
研究者成功合成了具有特殊3D结构的高度分支的Au超粒子,其独特的结构赋予其类似“黑体”的宽带吸收特性,能够高效吸收光线并转化为热量,为神经调控研究奠定材料基础。实验选用小鼠海马神经元细胞进行培养,采用钙离子成像和电生理记录等多种先进方法,全面评估该材料在神经网络中的应用潜力,并设置与传统Au纳米棒的对比实验。
结果显示,高度分支的Au超粒子光热转换性能卓越,效率超90%,而Au纳米棒仅为50%以下。这得益于其3D结构的广谱光吸收能力,可更有效捕获和利用光能。在光照刺激下,Au超粒子能有效引发神经元去极化,激发神经元活动。研究者通过精确调节光照强度,成功实现神经元活动的可逆调控,既能激发神经元产生放电活动,也能抑制其放电。
同时,实验表明Au超粒子生物相容性良好,在神经细胞培养过程中未观察到明显细胞毒性,对神经细胞正常生长和功能无不良影响。光热刺激引起的局部温度升高始终控制在神经元损伤的安全阈值之内,显示出该材料在神经调控应用中的安全性。
该研究通过对Au超粒子精心结构设计,显著提高其光热转换效率,并成功应用于非基因神经调控领域。这一新型纳米平台具备高空间和时间分辨率优势,能精确调控神经网络活动,为神经科学研究和神经工程领域发展开辟新途径,有望推动相关领域在疾病治疗、脑机接口等方面深入研究与应用。
清华大学化学系李景虹、张昊、生命学院姚骏、化学系瓮康康是本文的共同通讯作者。化学系2017级已毕业博士程昕予、化学系2021级博士生李文俊、生命学院2018级已毕业博士生王颖菡是本文的共同第一作者。清华大学化学系李景虹、张昊、生命学院姚骏、化学系瓮康康为共同通讯作者。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.4c07163
(二)金属有机框架修饰有机体异质结界面:突破非遗传神经调控瓶颈
尽管基于光热效应的金纳米材料在非遗传神经调控中展现出显著优势,其仍受限于材料-组织界面的适配性问题,尤其在实现高效、稳定且生物相容的神经刺激方面面临挑战。
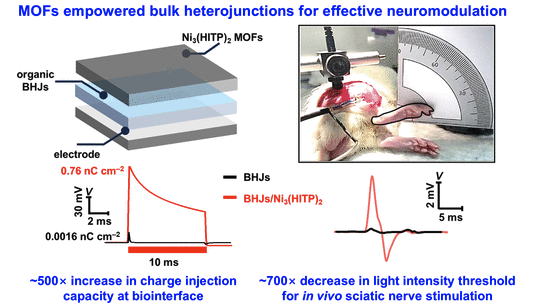
针对这一难题,清华大学化学系李景虹、张昊、电子工程系盛兴、生命学院姚骏共同通讯团队创新性地设计引入了由导电和多孔金属有机框架(MOF)组成的界面层。这一突破性设计有效应对了诸多挑战,为神经调控领域带来新曙光。相关研究成果以“金属-有机框架修饰有机体异质结界面用于有效的非遗传神经调节”(Metal–Organic Frameworks Modified Organic Bulk Heterojunction Interfaces for Effective Nongenetic Neuromodulation)为题在线发表于ACS Nano期刊。

研究团队选用的MOFs层成效显著。它使界面处的电荷注入能力提高了超过400倍,确保了BHJ与生物材料之间紧密且生物相容性的连接,支持在深红光和近红外光下对培养的小鼠海马神经元进行可靠的非遗传调节。由MOFs修饰的BHJ制成的柔性设备性能卓越,允许在超低光强度阈值(0.01 mW mm⁻⟡)下对大鼠坐骨神经进行体内刺激,这一阈值比未修饰设备所需的低700倍。
在生物相容性方面,MOFs凭借其负电性与纳米级粗糙表面,成功桥接了疏水光活性层与亲水聚赖氨酸涂层,使接触角从103°降至43°,成功支持小鼠原代海马神经元及大鼠背根神经节(DRG)神经元长期高活性生长,10天存活率超过95%。
功能验证环节,研究团队开展了多项严谨实验。基于大鼠DRG神经元的膜片钳实验证实了纯电容双向调控机制:低光强连续光(25 - 75 mW mm⁻⟡)能够诱导超极化抑制神经兴奋,而高光强脉冲(750 mW mm⁻⟡)则可触发钙离子介导的反弹去极化,且10 Hz脉冲激发成功率达到100%。活体实验进一步展示了该技术的优势,柔性器件包裹大鼠坐骨神经时刺激阈值大幅降低,近红外响应使PBDB - T:Y6器件光电压提升至75 mV,增幅达15倍。
本工作为神经调控领域构建了“材料 - 生物 - 电化学”协同新范式。该技术具备的双向调控能力为帕金森病震颤抑制与神经通路重建提供了精准工具。大鼠坐骨神经模型证实的超低能量刺激(0.04 mJ cm⁻⟡,较安全标准低3 - 4量级)为无创运动功能调控开辟了新路径。基于海马/DRG神经元的长期生物相容性验证及近红外深组织穿透特性,本研究为脑机接口与神经义肢开发奠定了技术基础,推动了植入式电子设备向高效能、高生物安全性及临床适用性的发展。
清华大学化学系李景虹、张昊、电子工程系盛兴、生命学院姚骏是本文的共同通讯作者。化学系已出站博士后瓮康康、化学系2021级博士生李文俊、化学系2017级已毕业博士程昕予、生命学院2024级博士生邢芸芸是本文的共同第一作者。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c01516