RNA干扰(RNAi)是许多真核生物中一种保守的RNA沉默机制, 小干扰RNA是RNA干扰的关键组成部分。在小RNA的加工过程中,Dicer家族蛋白起到了重要的作用,它们发挥作用的过程中常需要双链结合蛋白(dsRBP)作为辅因子来帮助它们发挥功能。在果蝇中,siRNA的产生是由ATP依赖型的Dicer-2(Dcr-2)蛋白在其辅因子Loqs-PD的辅助下,从长的双链RNA(dsRNA)上等距切割产生21个碱基对的双链siRNA。但是对于ATP依赖型的Dicer-2蛋白如何识别并切割RNA底物整个过程的分子机制仍不清楚。
2022年7月14日,清华大学生命科学学院王宏伟课题组与复旦大学麻锦彪课题组合作,在《自然》(Nature)杂志上发表了题为“果蝇Dicer-2/Loqs-PD处理双链RNA的结构机制”(Structural insights into dsRNA processing by Drosophila Dicer-2–Loqs-PD)的研究论文,通过冷冻电镜单颗粒技术解析了包括Dicer-2/Loqs-PD以及dsRNA的6个不同状态冷冻电镜结构(图1),并结合生化分析首次揭示了Dicer-2/Loqs-PD复合物结合并切割双链RNA产生siRNA的分子机制。
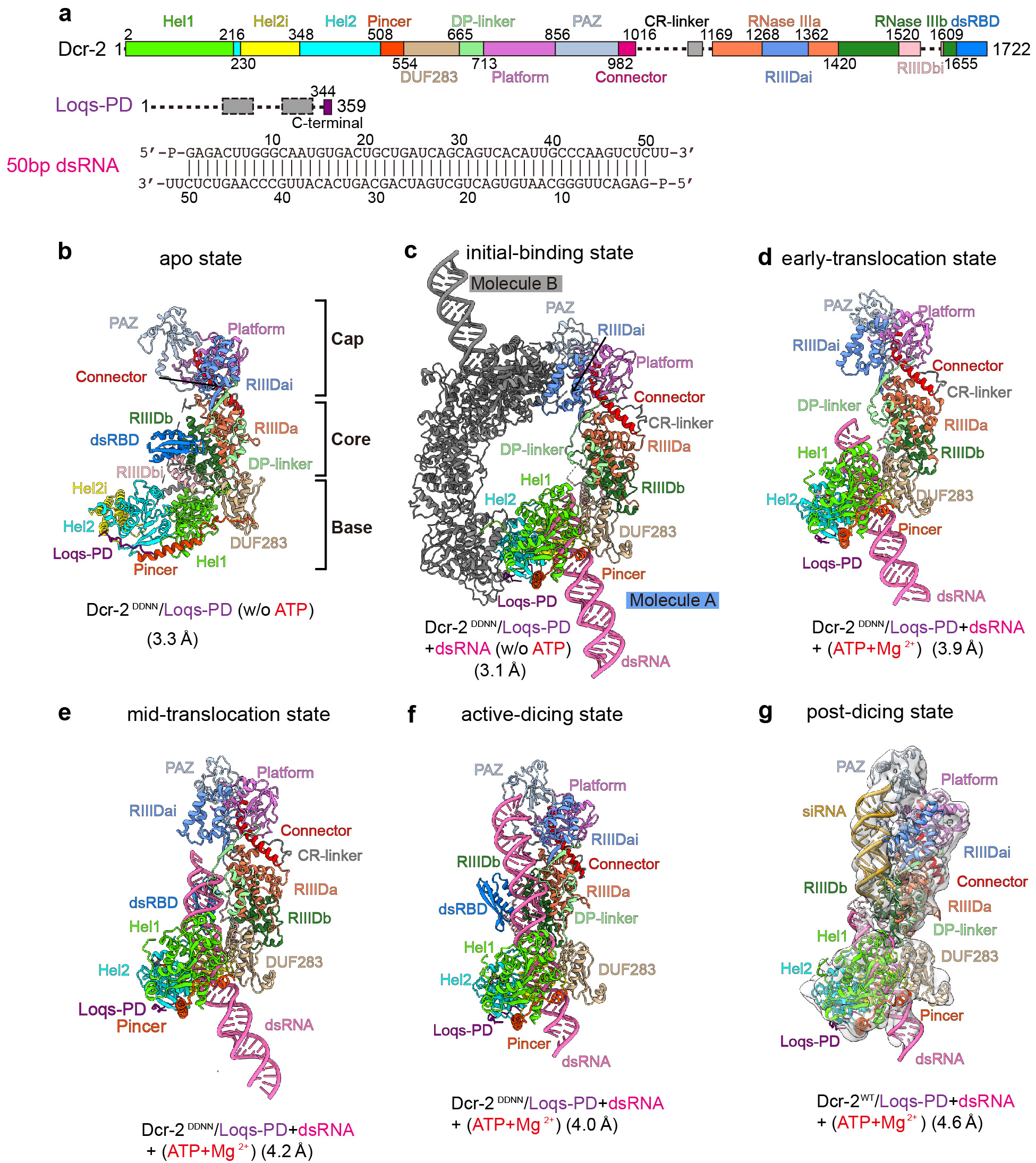
图1,Dicer-2/Loqs-PD复合物结构域示意图,以及结合双链RNA加工生成siRNA过程不同状态的冷冻电镜结构。
研究团队从活性位点突变的Dicer-2/Loqs-PD单独蛋白(apo)复合物结构开始解析。之后加入了双链RNA,获得了无ATP时,处在初始结合状态的Dicer-2/Loqs-PD–dsRNA复合物高分辨结构。发现在apo状态下松散的解旋酶结构域在初始结合状态中像手一样包裹住了双链RNA并扭曲了RNA的轴,此时解旋酶中的Hel1与Hel2亚结构域组成了成熟的ATP结合位点。在该状态下还明确了Loqs-PD主要通过C端与Dicer-2的解旋酶区域紧密结合的分子机制。在初始状态的基础上,进一步加入ATP和镁离子,通过数据收集与计算分类,得到了切割活性状态与两种明显具有不同结构特点的移位状态;与初始状态比较,两种移位状态中的Dicer-2–Loqs-PD复合物分别在双链RNA上移动了8bp和17bp左右,其中早期移位状态(~8bp)可以看作是在初始状态上的延伸,而中期移位状态(~17bp)中由于双链RNA穿过解旋酶的长度足够长,使得Dicer-2 C端的dsRBD结构域能够结合双链RNA,并对RNA的轴进行了进一步的偏转,使其指向能够识别末端PAZ-Platform结构域,RNA进一步的深入会使得其末端结合到PAZ-Platform结构域。之后,随着ATP水解导致的RNA进一步的深入、形变,从而产生的力使得解旋酶结构域以外的区域(cap-core区域)作为一个整体被RNA撑开,RNA进一步深入,最终到达切割活性状态,cap-core区域则紧密的结合在双链RNA上,确保精确的21bp siRNA的生成。之后研究者们使用正常活性的Dicer-2蛋白,获得了处于切割后状态的复合物,并通过分析发现它处于完成切割后正在回复到的早起移位状态的过程中。从而将整个过程串起,阐明了Dicer-2–Loqs-PD复合物从结合双链RNA并在其上移动,到形成切割活性状态,直至切割完成产生siRNA的整个循环过程的分子机制和其中连续且递进的构象变化。
清华大学生命学院王宏伟教授、复旦大学麻锦彪教授为论文共同通讯作者,复旦大学苏世晨博士和清华大学王家博士为论文共同第一作者,清华大学刘楠博士、李晓敏博士为样品制备和数据收集提供了重大帮助。国家蛋白质科学中心(北京)、清华大学冷冻电镜平台、清华大学高性能计算平台和水木未来(北京)科技有限公司为本研究提供了设备和技术支持。本研究得到了国家自然科学基金、国家重点研发计划、北京结构生物学高精尖创新中心、清华-北大生命科学联合中心以及Xplorer奖项等经费的支持。
论文链接:https://doi.org/10.1038/s41586-022-04911-x