动物可以通过听觉来敏锐的感受周围其他个体和环境的声音。听觉的产生有赖于耳蜗的精巧结构和功能,以及耳蜗中阶的内淋巴液的稳态。中阶内淋巴液为耳蜗提供能量物质的维持和代谢物质的转运,而耳蜗中阶内淋巴液的稳态失调是导致耳聋的最主要的因素。耳蜗中阶的内淋巴液是由血管纹组织所分泌并维持其成分,例如150毫摩的钾离子浓度和80毫伏的蜗内电位,因此血管纹的发生、发育和功能维持的研究有助于开发预防和治疗耳聋的方案。2021年10月5日,美国科学院院刊(PNAS)在线发表了清华-IDG/麦戈文脑科学研究院、清华大学生命学院熊巍课题组标题为“An L1 retrotransposon insertion induced deafness mouse model for studying the development and function of the cochlear stria vascularis”的研究论文,详细阐述了一株由逆转座子L1导致血管纹发育障碍的耳聋小鼠模型。
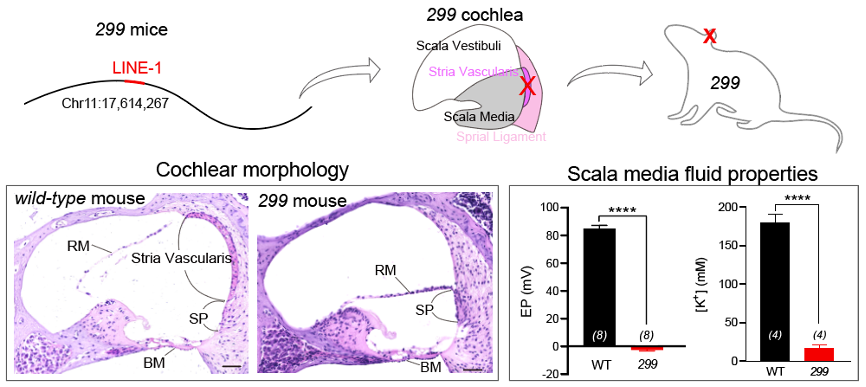
在本研究中,作者首先从ENU化学诱变小鼠种群里得到一株耳聋小鼠品系299,通过听觉电生理发现该小鼠品系的听性脑干电位和畸变产物耳声发射均完全丧失,而毛细胞电生理发现其机械转导功能维持正常。通过形态学观察发现该小鼠特异性的丧失了血管纹组织,进一步的在体电生理证明了耳蜗内淋巴液的蜗内电位和高钾浓度都消失了。
作者进一步鉴定了299小鼠的致病突变,通过二代测序并未发现相关突变,进一步的三代测序发现其致聋突变来自于一个大约7kb的逆转座子L1在第11号染色体上的插入。通过在299小鼠的第11号染色体上敲除该L1插入,从而挽救了299小鼠的耳聋表形,从而可以确定299小鼠的耳聋的确是由其11号染色体的L1插入导致。
基于该299小鼠,作者系统研究了耳蜗从胚胎期到听觉形成期的耳蜗结构和发育过程,以及血管纹的缺失对于毛细胞毛束形态和功能的影响。通过和野生型对照小鼠的耳蜗组织的转录组分析,作者进一步报道了和血管纹组织发育和功能相关的诸多基因,为后续的血管纹相关的研究奠定的基础。
综上所述,作者鉴定了一株耳聋小鼠品系299的致病突变和致病机理,利用一系列技术和方法,包括听觉电生理、毛细胞电生理、组织学、在体蜗内电位记录、小鼠遗传学和转录组测序分析等,鉴定了L1是229小鼠的致病突变,血管纹组织发育障碍是299小鼠的致病机制。该研究首次报道了一株逆转座子在非编码基因区导致耳聋的小鼠,揭示了血管纹发育的过程,提示了可能的血管纹发育和功能相关新基因,为研究L1基因调控功能和血管纹发育和功能提供了新的动物模型。
清华大学IDG/麦戈文脑科学研究院-生命学院熊巍研究员为本文的通讯作者,生命学院博士生宋晨萌和李杰为本文的共同第一作者。清华大学生命学院博士生刘双、侯函青、朱彤、陈姣凤、刘恋,清华大学医学院贾怡昌教授均为本研究做出了重要贡献。
原文链接:https://www.pnas.org/content/118/40/e2107933118