2018年10月4日,清华大学生命学院刘万里课题组在《科学》(Science)杂志发表题为《自身免疫病相关IgG1变异体调控B细胞活化及分化》(An autoimmune disease variant of IgG1 modulates B-cell activation and differentiation)的研究论文(First Release in an online article; the article will appear at a later date in print)。该论文首次报道人类膜联免疫球蛋白IgG1重链胞内区存在增加系统性红斑狼疮(SLE)易感性的单核苷酸多态性位点(SNP),并揭示该SNP参与调控B细胞命运决定的新机制,为研究系统性红斑狼疮等自身免疫疾病的致病机制和精准诊疗提供新的潜在靶点和理论支持。
SLE是最常见的自身免疫疾病之一,是一种由遗传、环境、免疫等多种因素导致的复杂性疾病,以产生多种自身抗体、免疫复合物沉积并累及多器官(皮肤、肾脏、肺脏、心脏和脑)为临床表现,造成一系列并发症,严重时可导致死亡。其发病机制至今尚不清楚,导致治疗手段有限且无法根治。因此探究SLE的发病机制一直是基础免疫学和风湿免疫病学关注的重点和难点。
B淋巴细胞是抗体免疫应答的核心效应细胞。在生理条件下,其通过分泌防护性抗体来清除入侵机体的病原体,从而保护人体的健康,并且留给人体记忆性免疫力,这也是B细胞通过疫苗免疫发挥防护效应的重要基础。然而,在病理条件下,具有自身反应性的B细胞在被异常激活后能够分泌识别自身抗原的抗体,这些自身抗体进而对自身组织进行攻击并引起抗体介导的免疫反应,并累及多个器官,对机体造成损害。具有自身反应性的IgG型记忆性B细胞在人体中广泛存在,而且SLE等自身免疫疾病常伴随大量自身抗体的产生。
基于上述两点事实,刘万里课题组提出IgG型B细胞受体(IgG-BCR)的异常活化可能参与到SLE等自身免疫病的发病过程中这一猜想。通过与北京大学人民医院牵头、北京大学深圳医院和北京大学第一医院参与的北大医学风湿免疫病学专业的合作研究,刘万里团队和栗占国团队共同发现人类膜联免疫球蛋白IgG1重链基因IGHG1上的SNP(rs117518546)在SLE患者中显著增加,该SNP导致人类膜联免疫球蛋白IgG1第396位甘氨酸突变为精氨酸(IgG1-G396R)。进一步的临床指标相关性分析表明,携带该SNP的SLE患者产生更多更广泛的IgG1型的自身抗体,发生炎症反应的风险增加,疾病活动指数也更高,揭示该SNP为新的SLE易感基因位点。有趣的是,刘万里团队通过分析千人基因组测序数据,发现该SNP主要在东亚人群中的携带频率(minor allele frequency,MAF)较高,而在欧美人群中极少,这提示该SNP是以汉族为代表的东亚人群特有的SLE易感基因位点,可能是我国SLE患者与其他人群患者的临床表现和治疗反应存在差异的因素之一。
刘万里团队进一步利用该SNP的基因敲入小鼠,发现在自身免疫诱导模型中,携带该SNP的小鼠产生更多、更广泛的自身抗体,而这依赖于B细胞受抗原刺激后大量自身反应性浆细胞的分化,从而验证了在SLE患者中的发现,并从B细胞命运决定层面给出了初步解释。与此同时,鉴于该SNP在东亚人种中的携带频率较高,且IgG型记忆性B细胞的产生和功能在疫苗免疫中发挥着重要作用,刘万里团队探索了该SNP对正常疫苗接种激发的抗体应答的影响。季节性流感疫苗免疫的健康志愿者队列研究揭示,该SNP的纯合型携带者的流感病毒特异性IgG1抗体应答显著高于未携带该SNP的健康志愿者。这一结果表明,该SNP对调控IgG型B细胞介导的抗体应答的具有典型的“双刃剑”效应:一方面促进机体中能识别非我抗原的防护性抗体的产生,帮助机体抵御病原体入侵;另一方面在免疫系统异常的情况下,促进识别机体自我抗原的记忆性B细胞产生自身抗体,加剧SLE的发生和发展。
在分子机理层面的研究中,刘万里团队发挥其实验室多年来的研究特色,整合基于全内反射荧光显微镜的高速高分辨率活细胞单分子成像平台和基于Matlab的单分子轨迹追踪算法,揭示该SNP显著延长IgG-BCR活化后招募的下游信号分子Grb2在B细胞免疫突触中的驻留时间。常规生化分析揭示这种增强的驻留特性,并非因为Grb2与SNP突变位点所在的磷酸化IgG-BCR胞内区免疫受体尾部酪氨酸基序(ITT-motif,以下简称ITT基序)的结合力增强。更进一步的基于激酶-底物互作的分子动力学模拟,揭示该SNP突变通过形成新的激酶-底物间的氨基酸残基相互作用(激酶290位天冬酰胺与底物390位精氨酸形成氢键),显著增强了Lyn激酶结构域与ITT基序的结合,进而极大的促进了Lyn对ITT基序的磷酸化效率,使得变异体的B细胞免疫突触中的磷酸化ITT基序的密度显著增加,从而改变Grb2在免疫突触中的招募模式,从招募-逃逸(Recruit and Escape),转换为招募-限制(Recruit and Confine), 这毫无疑问延长了Grb2在免疫突触中的停留时间,更有效促进Grb2-BTK-PLCγ2信号小体在免疫突触中的形成,极大的增强了包括NF-κB、Erk等在内的下游信号通路的免疫活化,上调Blimp1和Irf4等转录因子的表达,促进B细胞免疫活化后向分泌抗体的浆细胞分化的命运决定。
本论文从疾病易感基因位点的临床遗传学研究出发,开展大样本多中心临床相关性分析,再到基于基因修饰小鼠的动物模型研究,和基于新型成像技术和常规生化分析的受体活化信号通路解析,最后到基于分子动力学模拟的蛋白互作面的三维结构研究。这一系列的研究结果加深了人们对SLE易感基因位点功能及致病机理的认识,为SLE研究提供了全新的研究靶点,也为复杂疾病相关易感基因位点的研究提供了创新性的研究模式。值得一提的是,该研究发现了在以汉族人为代表的东亚人群中广泛存在,但在欧美人种中极少存在的SLE易感SNP,为在中国罹患SLE的近百万患者,提供精准医疗的潜在靶点和理论支持,具有重大的潜在的社会意义和经济价值,是书写在祖国大地上的研究成果。
清华大学生命学院2018年1月份已毕业的陈相军博士为论文第一作者,清华大学生命学院和免疫学研究所刘万里研究员为论文通讯作者,北京大学人民医院风湿免疫科栗占国教授为论文的共同通讯作者。北京大学人民医院风湿免疫科孙晓麟副研究员,清华大学生命学院PTN项目博士生杨为和清华大学生命学院博士生杨冰等为本论文研究做出重要贡献。本研究需要大力整合临床免疫学、基础免疫学、分子细胞生物学、生物物理学和计算生物学等不同学科的交叉优势,在研究过程中得到了北京大学定量生物学中心来鲁华教授,北京大学第一医院张宏教授,北京大学深圳医院王庆文教授,清华大学医学院和免疫所祁海教授,中科院上海生化细胞所许琛琦研究员,中科院生物物理所娄继忠研究员,中科院微生物所张福萍研究员,北京协和医院郑文洁教授,华中科技大学同济医学院郑芳教授,南京医科大学胡志斌教授等国内外同行的大力支持。该研究得到了清华大学实验动物中心、生物医学测试中心的支持。该研究由国家自然科学基金委、科技部、清华大学免疫学研究所、清华-北大生命科学联合中心、北京市科委和深圳市三名工程提供经费支持。
刘万里课题组一直致力于使用新型的高速高分辨率的活细胞单分子荧光成像技术,结合传统的分子免疫学、生物化学和生物物理学研究手段,对B淋巴细胞免疫识别、免疫活化及相关免疫疾病的致病机理进行研究。回国独立工作以来,以通讯作者(含共同)发表多篇论文:Cell、Leukemia、Science Immunology、J Exp Med、PNAS、eLife(2015和2017)、J Cell Biol、Nature Communications(2015和2017)、Science Signaling、Cell Research(2014和2018)、Cell Reports、J Immunol(2013、2014和2017)、Eur J Immunol.、Frontiers in Immunology、Trends ln Immunology等。该论文的发表是刘万里课题组对该领域的新贡献。据不完全统计,该论文也是国内科学家在B细胞免疫识别、免疫活化和免疫调控领域,在风湿免疫病研究领域,首次在《科学》(Science)杂志发表研究论文。
论文链接:http://science.sciencemag.org/content/early/2018/10/03/science.aap9310
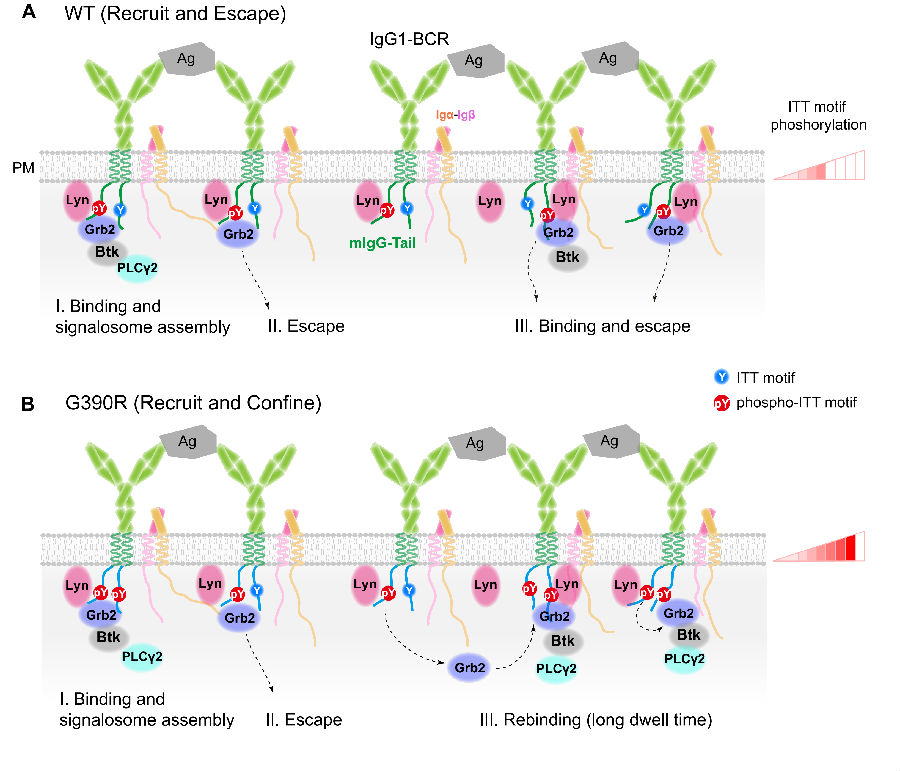
图1. SLE易感基因突变IgG1-G396R改变Grb2在B细胞免疫突触中的招募方式