2019年4月29日,清华大学生命学院颉伟研究组、上海交通大学李力研究组与中国科学院动物研究所李伟研究组通过紧密合作,在《自然-遗传》期刊以长文形式报道了题为《SETD2调控母源表观基因组、基因组印记以及早期胚胎发育》(SETD2 regulates the maternal epigenome, genomic imprinting and embryonic development)的研究论文,阐明表观遗传修饰之间如何通过相互作用建立卵子表观基因组包括基因印记,以及卵子表观基因组如何对早期胚胎发育产生重要影响。这一重要发现不仅阐明了母源表观基因组的建立机制和功能,还为将来临床评估卵母细胞质量以及探索早期发育相关疾病提供了新的研究方向。
在生命起始的时候,健康的卵母细胞对于胚胎早期发育是至关重要的。卵母细胞不仅提供了一半的DNA,而且提供了受精卵发育所必需的母源mRNA、蛋白质、细胞器等。另外,卵母细胞中的表观遗传信息如基因印记则保证了哺乳动物的两性繁殖。有趣的是,之前研究表明,哺乳动物卵母细胞具有独特的表观基因组。例如,DNA甲基化在小鼠卵母细胞中分布于活跃转录区域。而组蛋白修饰H3K4me3和H3K27me3则高度富集在转录抑制,具有DNA低甲基化的区域(Partially Methylated Domains, PMD)。然而这种独特的表观基因组在卵母细胞中是如何建立的,以及如何影响卵子发生和早期胚胎发育至今仍然知之甚少。
SETD2是一种组蛋白甲基转移酶,能够在组蛋白H3第36位赖氨酸上加上三个甲基化修饰(H3K36me3)。H3K36me3通常出现在转录活跃区域,被证明是一种由RNA 聚合酶转录时所带来的组蛋白修饰。在该研究中,研究人员首先利用颉伟课题组于2016年开发的高灵敏STAR ChIP-seq技术,系统地检测了小鼠卵母细胞与早期胚胎发育过程中H3K36me3的分布情况。研究人员发现,在小鼠卵母细胞中,H3K36me3与DNA甲基化呈现非常强的正相关性,而与H3K4me3以及H3K27me3则呈现互斥分布模式。随后,通过在卵母细胞中特异性敲除Setd2,研究人员发现该雌性小鼠具有不育特征。进一步研究发现,卵母细胞中表观遗传修饰的分布情况发生了巨大的改变,包含以下几个方面:1)H3K36me3在全基因组基本丢失;2)全基因组的DNA甲基化建立高度异常;3)母源基因印记完全丢失,同时这些区域错误的加上了拮抗DNA甲基化的H3K4me3。4)H3K4me3和H3K27me3被错误的建立在很多其他的转录活跃区域,其中H3K27me3的错误建立伴随着基因转录下调。与之同时,Setd2敲除卵母细胞排卵率下降,受精后早期胚胎发育阻滞在受精卵1细胞时期。为了进一步研究Setd2缺陷卵子如何造成早期胚胎发育阻滞,研究人员通过卵母细胞核质互换以及单精子显微注射受精的技术,揭示了Setd2母源缺陷的细胞质能够引起植入前胚胎发育阻滞,而染色质的缺陷则会导致植入后胚胎发育致死。因此,SETD2作为一个卵子表观基因组的核心调控因子,对确保卵母细胞表观基因组的正常建立,以及维持随后胚胎发育至关重要。综上所述,该研究系统地在小鼠卵母细胞发育过程中探索了表观基因组建立的分子机制,揭示了卵子表观基因组在卵子发生和早期胚胎发育过程中的重要功能。
颉伟教授、李力教授与李伟教授为本文的通讯作者,清华大学生命科学联合中心博士后徐倩华、博士研究生向云龙、清华大学生命学院博士研究生王秋军以及中国科学院动物研究所博士后王乐韵为本文共同第一作者。合作实验室包括英属哥伦比亚大学Matthew C. Lorincz研究组、Louis Lefebvre研究组与武汉大学吴旻研究组等。该课题得到了清华大学实验动物中心,生物医学测试中心基因测序平台以及计算平台的大力协助和支持。该研究获得了国家科技部重点研发计划、国家重点基础研究发展计划(973计划)、国家自然科学基金委杰出青年基金、北京市科技计划、清华北大生命科学联合中心以及美国霍华德休斯医学研究所国际研究学者(HHMI International Research Scholar) 的经费支持。
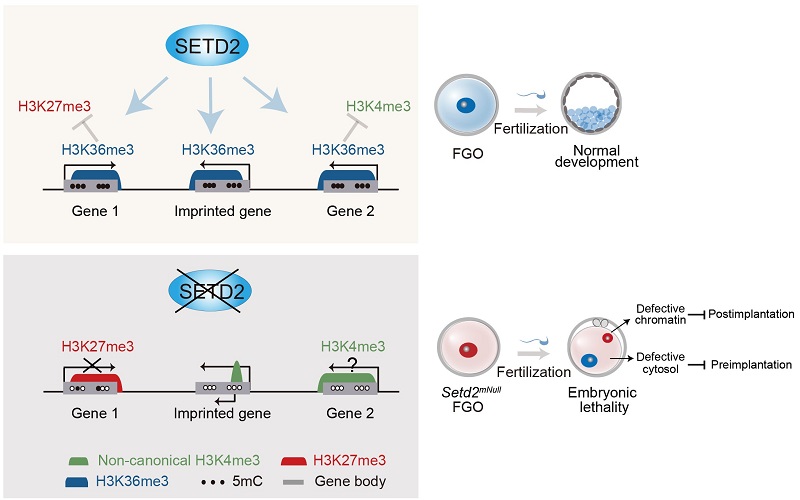
SETD2调控卵母细胞表观基因组、基因印记和早期胚胎发育
论文链接:https://www.nature.com/articles/s41588-019-0398-7